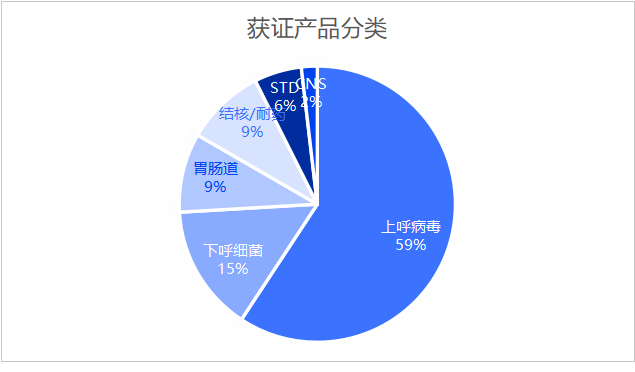
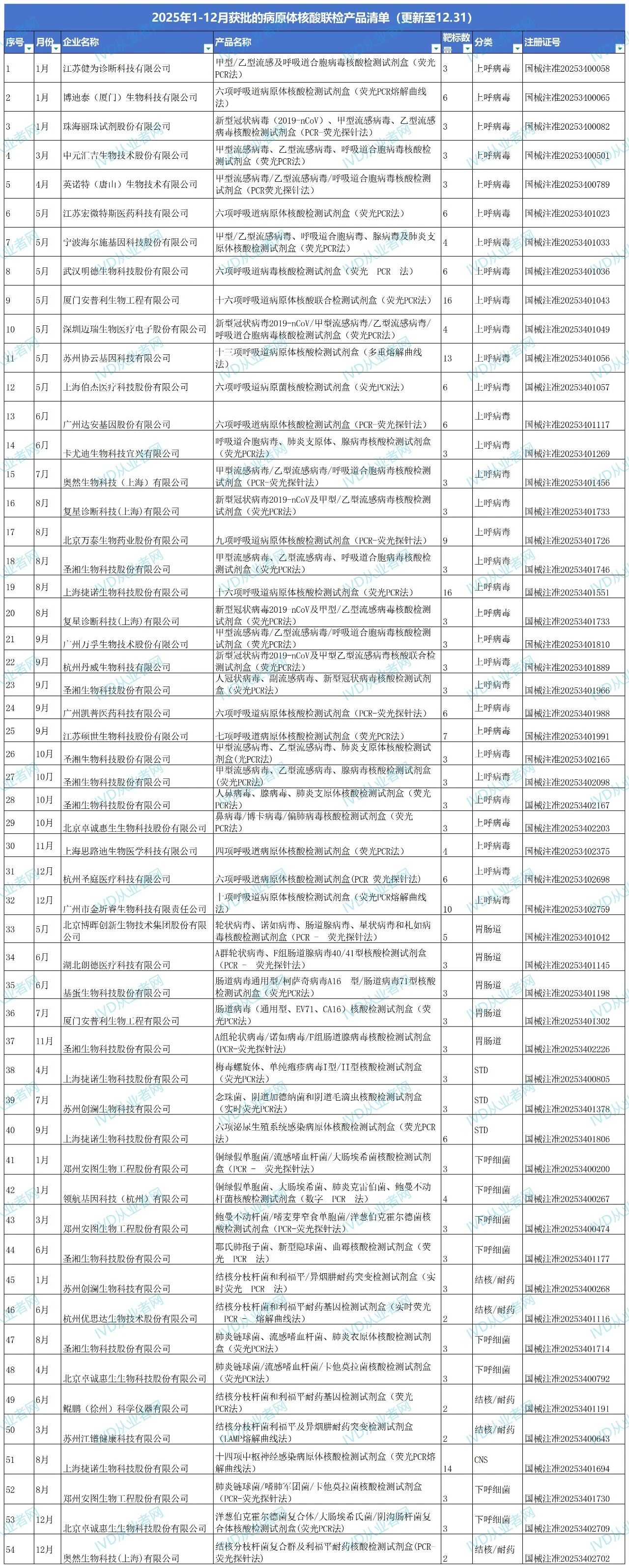
本报告基于国家药品监督管理局(NMPA)2025年度批准的54项多重核酸检测试剂产品注册数据,系统梳理了产品获批的时间分布、靶标通量、临床分类、企业格局及技术路线,剖析了我国多联检市场的现状、竞争态势与未来趋势。数据显示,上呼吸道病原体检测仍是绝对主赛道,3-6靶标的实用型产品占据主流,市场呈现“一超多强、多点开花”的竞争格局,技术平台在稳定的基础上持续创新。注:数据统计时,≥3重以上的病原体类、结核分枝杆菌及耐药联检统一记为核酸多联检。2025年,NMPA共批准多联检核酸检测产品54项。从临床分类看,市场高度集中于呼吸道感染领域,这契合了我国呼吸道传染病高发、临床快速鉴别诊断需求迫切的现状。- 上呼吸道病毒检测:32项,占总数的59.3%,是无可争议的核心赛道。
- 下呼吸道细菌/真菌检测:8项,占14.8%,关注院内常见致病菌及耐药菌。
- 胃肠道病原体检测:5项,占9.3%,主要针对病毒性腹泻病原。
- 结核及耐药检测:5项,占9.3%,聚焦快速分子药敏。
- 中枢神经系统(CNS)感染检测:1项,占1.9%,为技术门槛较高的细分领域。
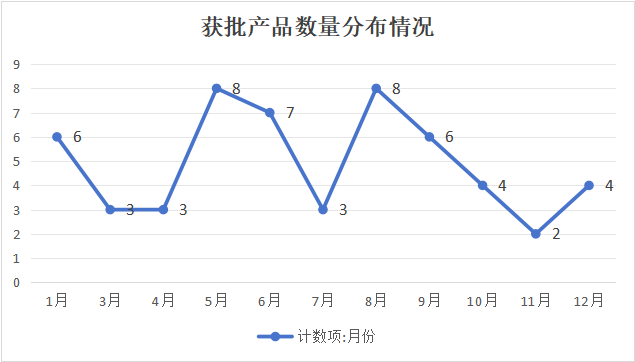
结论:产品布局紧密围绕重大公共卫生需求和临床常见感染症候群,呈现出显著的“需求驱动”特征。全年产品获批时间分布相对均匀,未出现长时间空窗期,反映了监管审评流程的成熟与稳定。- 平稳期:10月、12月(各4项),3月、4月、7月(各3项)。
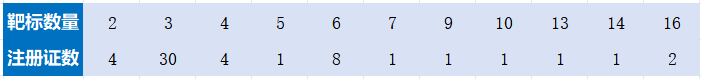
解读:5月、8月的获批高峰可能与企业在财年中期集中提交申报资料、以及审评资源周期性释放有关。全年“波浪式”的获批节奏,为企业研发和上市规划提供了可预期的监管环境。三、 靶标数量分析:“实用主义”主导,差异化竞争显现产品通量设计体现了市场在“检测广度”与“成本效率”之间的精准平衡。- 绝对主流(3靶标):30项,占比55.6%。此类产品通常组合临床最常见、症状最相似的病原体(如甲流/乙流/呼吸道合胞病毒),实现“精准快检”,满足门急诊核心需求,具有成本低、速度快、易推广的优势。
- 重要梯队(6靶标):8项,占比14.8%。覆盖更广谱的常见病原体,是平衡检测范围与成本的良好选择,尤其适用于儿童、老年患者等混合感染风险较高的人群。
- 高技术标杆:出现了16项(2款)、14项、13项、10项等超高通量产品。这些产品代表了企业的技术上限,主要定位于疑难病例筛查、流行病学监测或高端医疗市场。
- 其他靶标数量:4项(4款)、2项(4款)、以及7、9、5项等均有分布,显示企业在通量选择上进行着精细化的市场切割。
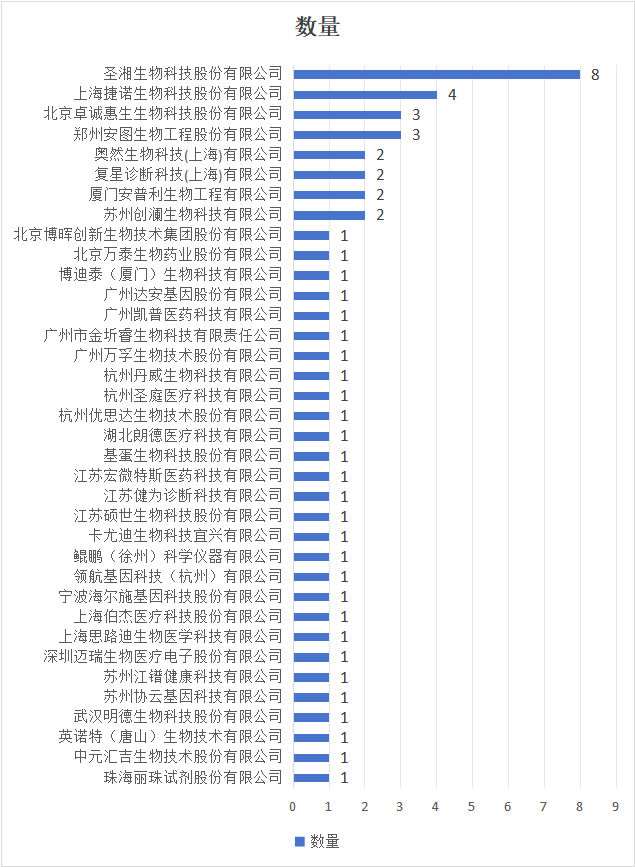
趋势洞察:市场并非盲目追求高通量,而是根据不同的临床场景(筛查、鉴别、确诊)和支付能力,形成了从“精准聚焦”到“全面筛查”的完整产品矩阵。54项产品来自39家企业,市场集中度与分散性并存。圣湘生物:以8项获批产品独占鳌头,产品线横跨上呼病毒、下呼细菌、胃肠道三大领域,展现了强大的研发管线布局和注册申报能力,龙头地位稳固。捷诺生物:获批4项,并在CNS(14项靶标)和STD(6项靶标)这两个高技术壁垒领域推出了重磅产品,体现了其在高难度细分市场的竞争优势。- 郑州安图生物(3项)、北京卓诚惠生(3项):专注于下呼吸道细菌检测,在院内感染病原体检测领域建立优势。
- 苏州创澜生物(2项):在STD和结核耐药检测领域持续投入。
多达31家企业仅获批1项产品。其中既有达安基因、迈瑞医疗、万孚生物、硕世生物等IVD知名企业,也有大量创新型生物科技公司。这表明:- 众多企业选择以单一差异化产品切入火热的市场,竞争异常激烈。
- 头部企业通过多产品线、全场景覆盖构筑了深厚的竞争护城河。
1. 技术平台:荧光PCR稳坐江山,新技术崭露头角- 荧光PCR/荧光探针法:仍是绝对主导技术(超过90%),因其成熟、稳定、成本可控。
- 熔解曲线法:在多项产品中应用,无需探针,有利于降低成本并实现多靶标检测。
- 创新技术试水:数字PCR(领航基因)、LAMP法(苏州江镨)等均有产品获批,虽然数量少,但代表了未来技术多元化的可能方向。
核心组合持续迭代:甲流/乙流/RSV仍是“黄金组合”,但企业通过加入腺病毒、肺炎支原体、鼻病毒、偏肺病毒、博卡病毒等,创造出更具临床针对性的新产品。“新冠+流感”联检需求延续:多家企业产品仍包含新型冠状病毒,满足常态化监测及混合感染鉴别需求。病原谱持续拓宽:16项、13项、10项等大通量产品不断挑战检测极限。下呼吸道检测:从常见菌向耐药菌(鲍曼不动杆菌)、真菌(耶氏肺孢子菌、曲霉)延伸。结核耐药:利福平+异烟肼双耐药检测成为主流,直接指导临床用药。胃肠道检测:覆盖轮状、诺如、肠道腺病毒等主要腹泻病毒。1. 驱动因素:新发突发传染病防控压力与医院降本增效(DRG/DIP支付改革)共同推动多联检市场扩张。一次检测鉴别多种病原体,符合临床和医保双重诉求。综合型企业(如圣湘):打造覆盖全感染领域的“产品航母”,提供整体解决方案。技术领先型企业(如捷诺):攻坚高技术壁垒的狭窄赛道(如CNS),建立专业壁垒。市场跟随者:通过更优的成本、渠道或某一点技术创新,在红海市场中寻找空间。通量两极发展:一方面,3项左右的“床旁化”、“快检化”产品需求旺盛;另一方面,20项以上的“超高通量”筛查产品将继续作为技术标杆存在。技术融合:微流控、全自动化、人工智能结果判读等技术将与多联检结合,提升检测便捷性与智能化水平。监管与标准化:随着产品复杂度提升,建立统一的性能评价标准、参考品和质控体系将成为行业健康发展的关键。2025年的多联检市场数据描绘出一幅“需求明确、技术务实、竞争激烈、创新不断”的行业图景。上呼吸道检测是主战场,但细分市场的专业化竞争已然打响。圣湘生物凭借全面的管线布局确立了领先优势,而众多企业则在各自擅长的领域寻求突破。展望未来,市场增长动力依然强劲。企业能否成功,取决于其是否能精准把握临床未满足的需求、持续进行技术创新、并构建差异化的市场与商业能力。对于整个行业而言,在追求“更多、更快”的同时,确保“更准、更稳”,并推动临床应用的规范化,将是实现可持续发展的基石。声明:本微信注明来源的稿件均为转载,仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正。