2025年是中国发现首例HIV感染者40周年。在这四十年间,中国艾滋病检测技术经历了从无到有、从引进到自主创新的跨越式发展。近日,《中国艾滋病性病》杂志发表了一篇题为《我国艾滋病检测技术和检测产品的发展与现状》的综述文章,系统梳理了我国HIV检测技术的演进路径与产业现状。

作为IVD行业的观察者,我们从中看到了一个清晰的技术演进图谱,也看到了国产IVD企业在艾滋病检测领域的持续突破。
从ELISA到化学发光:国产试剂的四次迭代
文章指出,我国HIV抗原抗体检测技术已从第一代ELISA发展到第四代联合检测试剂,窗口期从40-50天缩短至14天左右。1989年,中国预防医学科学院研制出首款国产HIV ELISA试剂;2004年,国内首个第四代HIV抗原抗体联合检测试剂获批上市,标志着我国在血清学检测领域实现了从“跟跑”到“并跑”的转变。
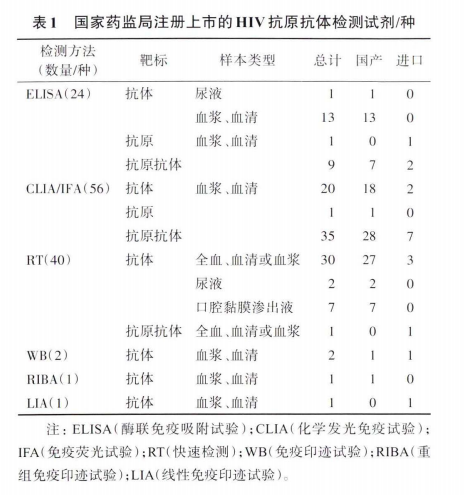
截至目前,国家药监局已累计注册上市124种HIV抗原抗体检测试剂,其中国产试剂占据绝大多数。化学发光检测(CLIA)因其高灵敏度、自动化程度高等优势,正在成为HIV筛查的主流平台,国产CLIA试剂也在逐步替代进口产品。
自我检测的“中国方案”:尿液自检试剂全球首发
2019年,我国自主研发的全球首个以尿液为标本的HIV自我检测试剂盒获批上市,成为HIV自检领域的“中国名片”。这一突破不仅拓宽了检测场景,也为高危人群提供了更隐私、更便捷的检测方式。
目前,国内通过电商平台销售的HIV快速检测试剂品牌已达34种,形成了覆盖线上线下的自检网络。2019年发布的《艾滋病自我检测指导手册》也为自检提供了标准化操作指引。
核酸检测:从定性到定量,国产试剂性能已不输进口
在核酸检测领域,我国已上市21种HIV-1核酸检测试剂,涵盖RNA定量、RNA定性、DNA定量等多种类型。2002年,首个国产HIV荧光PCR试剂获批;2024年,首个基于qPCR的HIV-1 DNA定量检测试剂获批,为抗病毒治疗效果评估提供了新工具。
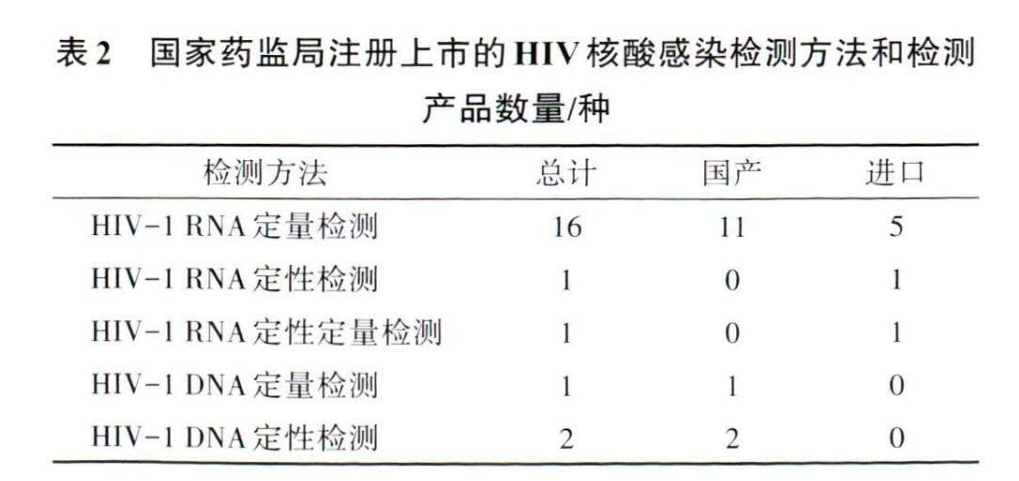
值得注意的是,国家艾滋病参比实验室的研究显示,国产HIV病毒载量试剂与进口试剂在检测结果上具有高度一致性和相关性,部分国产试剂在性能上已具备替代进口的能力。
耐药检测:从实验室自建到产品化落地
HIV耐药检测是实现个体化治疗的关键。近年来,基于Sanger测序的HIV耐药检测试剂已实现国产化,2024年国内首款HIV-1耐药检测试剂获批上市。同时,基于二代测序(NGS)和三代测序(TGS)的耐药检测技术也在快速发展,未来有望实现高通量、高灵敏度的耐药突变检测。
免疫功能检测:国产流式细胞仪崛起
CD4细胞计数是评估HIV感染者免疫状态的核心指标。截至2025年9月,国家药监局已批准55种国产流式细胞仪和20种国产CD4检测试剂,国产仪器在性能和稳定性上已与进口产品相当,显著降低了实验室检测成本。
展望未来:更早、更准、更便捷
文章指出,未来HIV检测技术的研发将向“更早、更准、更快、更便捷、更智能、更普惠”方向发展。第五代筛查技术、POCT核酸快速检测、微流控、CRISPR等新兴技术正在加速落地,有望进一步缩短窗口期、提升检测可及性。
从1989年首款国产ELISA试剂,到2024年首款HIV耐药检测试剂获批,再到全球首创的尿液自检试剂,中国艾滋病检测产业已走出一条从引进、消化、吸收到自主创新的完整路径。对于IVD从业者而言,这不仅是一个市场的成长史,更是一个行业责任的体现。未来,随着新技术的不断落地,中国IVD企业有望在全球HIV检测市场中扮演更加重要的角色。






